Комплекс поражений почечных структур при сахарном диабете носит название диабетической нефропатии. Негативные влияния на сосуды почек и состояние клубочковой фильтрации имеют место с момента манифестации болезни.
Темпы прогрессирования патологии почек при диабете во многом определяются степенью компенсации нарушений углеводного обмена и контролем уровня артериального давления. На стадии уремии больные нуждаются в гемодиализе или трансплантации почки.
В индустриальных странах сахарным диабетом страдает до 5–10% населения. Исследователи отмечают тенденцию к повышению распространенности болезни. Одной из серьезных проблем считается диабетическая нефропатия, в финале приводящая к почечной недостаточности.
Поражение почек наблюдается в среднем у 40% пациентов. Нефропатия характерна для диабета любого типа. При этом у больных с 1 типом заболевания это осложнение является одной из главных причин ранней инвалидности и смертности.
Варианты диабетического поражения почек
Нефропатия при диабете – это целый комплекс изменений в артериях, клубочках, канальцевом аппарате, связанный с метаболическими нарушениями, изменениями гемодинамики, локальным повышением активности ренин-ангиотензиновой системы, генетическими факторами.
Распространенным вариантом диабетического поражения почек является гломерулосклероз. Он может быть диффузным, экссудативным, узелковым. Последняя форма специфична для сахарного диабета, обычно выявляется при 1 типе заболевания.
Помимо гломерулосклероза при диабетическом повреждении почек могут наблюдаться артериолосклероз, склероз почечной артерии, отложения липидов, полисахаридов, гликогена в области канальцев. Поиск вариантов патологии помогает в разработке эффективных методов профилактики и терапии.
Патогенез формирования диабетической нефропатии
Существует ряд теорий возникновения диабетического поражения почек. Наиболее изучены 3 теории, описывающие разные пусковые факторы развития патологии:
- повреждение структур почек вследствие метаболических сдвигов,
- негативное влияние гемодинамических нарушений,
- реализация генетической предрасположенности.
Хроническая гипергликемия приводит к гиперфильтрации и внутриклубочковой гипертензии. Давление в клубочках определяется несколькими факторами, в том числе разницей диаметров входящего и отводящего сосудов.
Первый примерно в 2 раза шире второго. Метаболические нарушения, в первую очередь повышенные концентрации сахара крови, вызывают приток жидкости в кровеносное русло, снижение эластичности сосудистой стенки и, как следствие, увеличение диаметра входящих артериол.
Высокий сахар крови ведет к дополнительному повреждению эндотелия сосудов свободными радикалами. При этом защитные белки подвергаются гликированию и теряют свои антиоксидантные свойства.
Еще один важный фактор возникновения диабетической нефропатии – чрезвычайно высокая активность ренин-ангиотензиновой системы в почечной ткани. Огромные концентрации ангиотензина 2 приводят к повышению давления в клубочках за счет спазма выносящей артериолы.
Кроме того, вещество способствует склерозированию тканей и структур.
Генетическая предрасположенность определяет развитие начальных этапов болезни. Одни типы полиморфизма генов АПФ и NO-синтетазы предрасполагают к формированию патологии почек, а другие предохраняют от нее. На стадии протеинурии генетические факторы уже не имеют существенного значения.
На первый план среди причин прогрессирования болезни и появления тяжелой почечной недостаточности выходит уровень контроля артериального давления.
Гипертензия непосредственно влияет на давление внутри клубочков, влияя на скорость фильтрации крови. В итоге через гломерулярный барьер проникают белки, липиды, форменные элементы крови. Длительное повышение давления в клубочках вызывает их деструкцию и склерозирование.
Формированию диабетической нефропатии способствует высокобелковая диета. Количество белка в рационе должно быть нормальным, а при развитии недостаточности его потребление необходимо снизить. Высокобелковая диета способствует усилению патологических процессов:
- росту давления и фильтрации в клубочках;
- протеинурии, скоплению белков и липидов в почечных структурах;
- возникновению ацидоза вследствие избытка азотистых шлаков;
- повышенной активации факторов роста и прогрессированию склеротических процессов.
Поиск и исследование механизмов прогрессирования патологии значительно повысили эффективность методов профилактики и терапии этого тяжелого осложнения диабета. Не так давно нефропатию диагностировали и начинали лечить лишь на стадии клинических проявлений.
В настоящее время серьезное внимание уделяется выявлению доклинических маркеров диабетического поражения почек. Одним из основных показателей начала функциональных и структурных повреждений клубочкового аппарата является микроальбуминурия.
Стадии
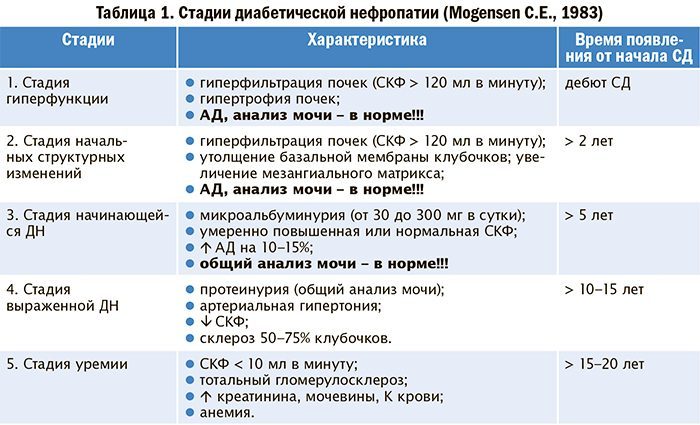
На современном этапе выделяют 5 стадий развития болезни. Первые три отображают доклинические изменения морфологии и функционирования почек. Последние две стадии соответствуют выраженным клиническим проявлениям диабетической патологии.
Стадии нефропатии:
- На первой стадии наблюдается острая гипертрофия и гиперфункция клубочков. При тщательном обследовании можно выявить повышение кровотока и скорости клубочковой фильтрации. Эти изменения при адекватном лечении диабета полностью обратимы.
- Для второй стадии – нормоальбуминурической, характерно появление начальных структурных повреждений артерий и базальных мембран клубочков. Экскреция альбуминов в пределах нормы, но постепенно нарастает, увеличиваясь примерно на 20% ежегодно.
- На третьей стадии – начинающейся, появляется микроальбуминурия. Для нее характерно повышенное содержание альбуминов в суточной моче (30–300 мг). Помимо морфологических изменений клубочков на этой стадии специальные методы исследования могут показать повреждение канальцевых структур.
- Для четвертой стадии характерна выраженная нефропатия. Клинически она проявляется протеинурией, гипертензией, отеками. В крови выявляется анемия, связанная с недостатком эритропоэтина.
- Пятая стадия – уремическая. Почечная недостаточность характеризуется снижением клубочковой фильтрации. Появляются симптомы интоксикации из-за скопления продуктов обмена в крови. Развивается примерно через 20 лет от дебюта заболевания или спустя 5–7 лет от начала протеинурии.
На первых трех стадиях можно добиться восстановления плазмотока и нормализации проницаемости сосудов клубочков. Для этого следует поддерживать в норме сахар крови и системное давление. Повышенная проницаемость для альбуминов связана также с ангиопатией и повышенным холестерином крови.
Клиника
Особенностью первых трех доклинических стадий заболевания является отсутствие жалоб и каких-либо клинических проявлений болезни. Обычные исследования также могут не показать структурных и функциональных изменений в почках на этом этапе болезни.
Показатели креатинина, мочевины крови остаются в пределах нормы. Поиск микроальбуминурии требует использования специальных методик проведения анализа.
Клинические симптомы появляются на стадии выраженной нефропатии. К ним относятся:
- Протеинурия (выделение белка свыше 500 мг за сутки). Осадок мочи обычно не меняется.
- Отеки, появляющиеся вначале на лице и голенях, впоследствии распространяющиеся на другие участки и полости тела. Жидкость может накапливаться в брюшной, плевральной, перикардиальной полостях. Отеки устойчивы к терапии диуретиками.
- Повышенное артериальное давление.
- Скорость клубочковой фильтрации начинает снижаться, уменьшается почечный плазмоток.
- Повышенный уровень креатинина, мочевины крови. Начало и прогрессирование почечной недостаточности.
- Слабость, одышка при скоплении жидкости в полости плевры, присоединение или усиление сердечной недостаточности.
- При диабете нефропатия обычно сопровождается признаками полинейропатии, ретинопатии, ишемической болезни сердца.
- Анемия смешанного генеза.
При наступлении уремической стадии болезни наблюдается нарастание симптомов почечной недостаточности: прогрессирует артериальная гипертензия, отечный синдром усиливается вплоть до анасарки, беспокоит одышка, учащенное сердцебиение, может развиться отек легких.
Для этого этапа характерно еще большее снижение уровня гемоглобина крови.
Уремия сопровождается скоплением токсических соединений в крови. На фоне выраженной интоксикации возникают зуд, появляется сухость и дряблость кожи, запах аммиака изо рта, рвота, развивается энцефалопатия. В тяжелых случаях выявляют шум трения перикарда.
Определение клубочковой фильтрации показывает значительное снижение показателя – менее 10 мл/мин.
Диагностика
Для выявления начальных этапов патологии почек определяют скорость клубочковой фильтрации и наличие микроальбуминурии. Скрининг должен проводиться не реже раза в год. Поиск минимальных изменений функционирования почек при диабете необходим для своевременного оказания помощи пациентам и предотвращения прогрессирования болезни.
Существует несколько методов определения суточной экскреции альбуминов: анализ уровня белка в моче, собранной за сутки, за ночь или же в утренней порции мочи. В утренней моче подсчитывают отношение концентрации альбумина к содержанию креатинина.
Такая методика более удобна и показывает довольно точные результаты, поскольку рассчитываемое соотношение коррелирует с уровнем экскреции белков в течение суток.
Скорость фильтрации в клубочках определяют по специальным формулам. Для расчета параметра пользуются значениями креатинина крови или клиренсом экзогенных препаратов. Фильтрационная функция почек показывает стадию диабетической нефропатии.
На начальных этапах показатель возрастает в 2 и более раз – до 300 мл/мин. Развитие почечной недостаточности приводит к снижению скорости. В уремическую стадию параметр падает значительно ниже нормального уровня (7–10 мл в минуту и меньше).
Анализ мочи включает обязательное определение количества форменных элементов крови. В ходе диагностики необходимо исключить нефрит другого происхождения. Патология почек может быть вызвана воспалительными или аутоиммунными причинами.
В спорных ситуациях может понадобиться чрескожная биопсия. Выявленные в биоптате патологические изменения должны показать характер имеющегося поражения почек.
Кроме того, при диабетической нефропатии анализируют уровни креатинина, мочевины крови. Канальцевые повреждения при диабете может показать определение активности органоспецифических ферментов.
На данный момент продолжается поиск новых эффективных методов диагностики ранних этапов поражения почек при диабете. Одной из перспективных методик является выявление генетической предрасположенности к патологии.
Лечение при диабете
Основной задачей лечения диабетической патологии почек является поддержание нормальных уровней сахара крови и гликозилированного гемоглобина. Это достигается правильным подбором дозы и режима введения инсулина при первом типе диабета.
Адекватность инсулинотерапии контролируется определением уровня гликозилированного гемоглобина, который должен быть не более 7%. При втором типе диабета, если показатели не соответствуют целевым, к терапии пероральными сахароснижающими средствами добавляют инсулинотерапию.
Ингибиторы ангиотензинпревращающего фермента показаны не только при гипертензии, но и при нормальном давлении. В последнем случае назначают низкую дозу препарата. За счет терапии удается нормализовать показатель и устранить негативное влияние активации ренин-ангиотензиновой системы.
Результатом будет замедление прогрессирования диабетического поражения почек.
Давление необходимо поддерживать на нормальном уровне, не более 130/85 мм рт. ст. В комплексную терапию следует включить мочегонные препараты. При необходимости врач проводит поиск оптимальной схемы лечения гипертензии, позволяющей достигнуть целевых значений.
Для нормализации липидного состава крови назначают диету, рекомендуют увеличить физические нагрузки, отказаться от вредных привычек. Если модификация образа жизни не нормализует показатели холестерина и липопротеидов, назначают статины или фибраты.
При развитии уремии в комплекс мероприятий включают симптоматическую терапию: нормализацию электролитного баланса, дезинтоксикационную терапию. Повышение креатинина крови выше 500 мкмоль/л – показание для гемодиализа и поиска альтернативных методов решения проблемы, в частности, трансплантации почки.
Поиск новых препаратов, обладающих способностью уменьшить повреждение тканевых структур почек, продолжается. Проводятся исследования эффективности применения таких лекарственных средств, как Вессел Дуэ Ф, аминогуанидина.
Профилактика диабетической почечной патологии
Оптимальная компенсация сахарного диабета – не только лежит основа терапии на любой стадии болезни, но и главный способ профилактики диабетической нефропатии. Вторым важным условием предупреждения прогрессирования патологии является нормализация уровня артериального давления.
Первичная профилактика
Профилактика нефропатии должна начинаться с общих мер, таких как активный здоровый образ жизни, правильный режим дня, процедуры закаливания, профилактика инфекций. Рекомендуется избегать вредных привычек, в частности, курения, употребления алкоголя и других.
Целью профилактики является предотвращение микроальбуминурии. Помимо компенсации диабета и поддержания оптимального уровня кровяного давления, внимание следует уделить коррекции липидного состава крови, соблюдению диетических рекомендаций, режима питания и физических нагрузок.
Вторичная профилактика
По мере прогрессирования заболевания пациенту необходимо строгое соблюдение диеты с ограничением приема не только углеводов, но и животных жиров, холестерина. Рацион не должен содержать большого количества белка, а при наличии симптомов снижения скорости клубочковой фильтрации употребление белковой пищи следует ограничить (под врачебным контролем).
Объем выпиваемой жидкости уменьшают при появлении отеков. Ограничение соли необходимо с самого начала развития гипертензии.
Следует строго контролировать показатели сахара крови и артериального давления, не допуская их повышения. Для нормализации гемодинамики почек показано назначение блокаторов ренин-ангиотензиновой системы.
Дорогие друзья. Данный материал не является медицинским советом, за диагнозом и способом лечения, обратитесь к специалисту для консультации.